引言 Introduction
醫(yī)用鈦合金生物性能優(yōu)異,耐腐蝕性好,比強(qiáng)度高,耐疲勞性好,生物相容性極佳,且力學(xué)性質(zhì)接近人體骨骼,已廣泛用于個(gè)性化醫(yī)療領(lǐng)域。據(jù)統(tǒng)計(jì),2014至2016年,鈦加工材料在醫(yī)藥領(lǐng)域的應(yīng)用分別達(dá)到了698噸、884噸和1 834噸,其中2016年的增長率高達(dá)107%[1]。隨著越來越多的試驗(yàn)研究和臨床應(yīng)用,鈦合金在牙科和骨科材料方面的應(yīng)用越來越具有突出的優(yōu)越性。在牙科領(lǐng)域,鈦及鈦合金廣泛用來制作冠橋修復(fù)體、牙種植體、義齒支架、正畸弓絲、種植體基臺(tái)、鈦板、鈦釘、正畸支抗釘?shù)萚2-3]。在骨科領(lǐng)域,鈦合金也得到了廣泛應(yīng)用,是生產(chǎn)人工關(guān)節(jié)假體(如髖、膝、踝、肩、肘、腕、指關(guān)節(jié)等)、骨接合產(chǎn)品、骨創(chuàng)傷產(chǎn)品(如螺釘、鋼板、骨髓內(nèi)釘?shù)?和脊柱內(nèi)固定系統(tǒng)的理想材料[4-5]。
傳統(tǒng)的鈦合金加工方法主要采用鑄造工藝,但鑄造工藝存在很多縮孔、內(nèi)孔、表面粗糙不光潔、龜裂、精度差等問題,很難滿足當(dāng)前個(gè)性化醫(yī)療的高要求。另外,鈦及鈦合金屬于高活性、易氧化的金屬合金材料,制作環(huán)境要求嚴(yán)苛,生產(chǎn)成本很高。因此,迫切需要開發(fā)新的生產(chǎn)技術(shù)來彌補(bǔ)傳統(tǒng)制造方法的不足。3D打印激光快速成型技術(shù)具有諸多優(yōu)點(diǎn),如生產(chǎn)周期短、制造精度高、工藝簡單便捷等,有效彌補(bǔ)了傳統(tǒng)鑄造工藝的不足[6]。
金屬3D打印是一種基于激光、電子束等熱源熔化金屬粉末的快速制造技術(shù),能夠成型復(fù)雜形狀零件,進(jìn)行個(gè)性化定制服務(wù),成型精度高、節(jié)約材料,對(duì)于復(fù)雜物品具有很高的成本優(yōu)勢(shì),并且簡化了生產(chǎn)流程,生產(chǎn)過程中節(jié)能環(huán)保,在醫(yī)學(xué)領(lǐng)域的應(yīng)用優(yōu)勢(shì)已經(jīng)漸漸凸顯。
目前,制備純鈦和鈦合金的3D打印技術(shù)主要有電子束熔化(electron beam melting,EBM)、選區(qū)激光熔化(selective laser melting , SLM) 和 選 區(qū) 激 光 燒 結(jié)(selective laser sintering,SLS)。3種技術(shù)原理大致相同,但存在差異。SLS加工前需要使用高分子聚合物或低熔點(diǎn)金屬作為粘結(jié)材料,燒結(jié)過程中才能與高熔點(diǎn)金屬相融合。因而該技術(shù)加工步驟很繁瑣,成型過程中的各種因素都會(huì)極大地影響零件精度[7]。因而在SLS技術(shù)的基礎(chǔ)上誕生的SLM技術(shù)更適合用于鈦合金的打印。而SLM和EBM都是以高能束流為熱源,選擇性地熔化金屬粉末而成型,工作原理大致為:鋪粉裝置在加工倉上鋪上一層金屬粉末,根據(jù)每一層的切片數(shù)據(jù),加工熱源選擇性地熔化金屬粉末,得到成型零件的每一層形狀,然
后加工倉下降一層,鋪粉裝置再鋪一層金屬粉末,熱源再繼續(xù)熔化該層粉末,如此逐層累積,最終得到成型的金屬零件。不同的是,SLM采用激光為熱源,在惰性氣體條件下熔化成形;EBM采用電子束為熱源,在真空條件下熔化成形。兩種工藝各有各的特點(diǎn)和優(yōu)勢(shì),分別可應(yīng)用在不同的領(lǐng)域。
目前很多學(xué)者都在致力于研究3D打印技術(shù)用于個(gè)性化醫(yī)療領(lǐng)域的適宜性。劉一帆等[8]應(yīng)用SLM工藝生產(chǎn)鈦合金可摘局部義齒支架,并對(duì)其適合性進(jìn)行研究,指出SLM技術(shù)制作的鈦合金可摘局部義齒支架的適合性基本滿足臨床要求。陳光霞等[9]針對(duì)傳統(tǒng)制造方法在鈦及鈦合金可摘除局部義齒支架制造中的不足,使用自主開發(fā)的SLM快速成型設(shè)備及相關(guān)的軟件控制系統(tǒng)生產(chǎn)義齒支架,并進(jìn)行了大量的工藝試驗(yàn)研究,不斷優(yōu)化工藝參數(shù),制造出鈦合金可摘除局部義齒支架。證實(shí)SLM技術(shù)完全可以滿足鈦及鈦合金支架的生產(chǎn)要求。
由于新興的3D打印技術(shù)的操作流程與傳統(tǒng)的加工過程存在較大差異,3D打印技術(shù)生產(chǎn)的鈦及鈦合金產(chǎn)品是否具備生物醫(yī)用材料所需要的安全性是業(yè)界普遍關(guān)注的問題。生物醫(yī)用材料用于人體時(shí),不能引發(fā)材料結(jié)構(gòu)和性能發(fā)生質(zhì)變,醫(yī)用材料與組織器官的反應(yīng)應(yīng)處于可接受的水平,不應(yīng)引起人體細(xì)胞、血液和器官發(fā)生過敏、炎癥及化學(xué)等不利反應(yīng),不能出現(xiàn)人體異物排斥反應(yīng)[10]。為了更好地研究3D打印技術(shù)在數(shù)字化、定制化及個(gè)性化醫(yī)療領(lǐng)域的應(yīng)用,文獻(xiàn)分析了3D打印鈦及鈦合金在耐腐蝕性、生物相容性方面的研究進(jìn)展,以更好地評(píng)價(jià)其生物安全性,為3D打印鈦及鈦合金在下一步的臨床應(yīng)用提供參考依據(jù)。
1、 資料和方法 Data and methods
1.1 資料來源
作者應(yīng)用計(jì)算機(jī)檢索中國知網(wǎng)、萬方數(shù)據(jù)庫,檢索時(shí)間為1980年至2018年1月,檢索關(guān)鍵詞為“3D打印;選區(qū)激光熔化;電子束熔化;選區(qū)激光燒結(jié);SLM;EBM;SLS;鈦;鈦合金;Ti-6Al-4V;耐腐蝕;生物相容性;3D printing;biocompatibility;selectivelaser melting;selective laser sintering;electron beammelting”等。
1.2 入選標(biāo)準(zhǔn)
納入標(biāo)準(zhǔn):3D打印鈦及鈦合金生物相容性、生物安全性、耐腐蝕性方面的原創(chuàng)性試驗(yàn)研究文獻(xiàn)。
排除標(biāo)準(zhǔn):非原創(chuàng)性研究文獻(xiàn)、綜述。
1.3 數(shù)據(jù)提取與質(zhì)量評(píng)價(jià)
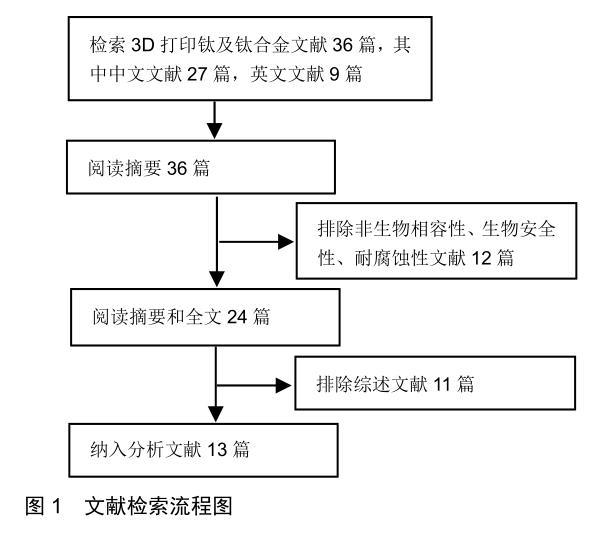
共獲得13篇文獻(xiàn)對(duì)3D打印鈦及鈦合金的生物安全性進(jìn)行研究[11-23]。其中文獻(xiàn)[11-12]為3D打印純鈦的生物相容性研究,文獻(xiàn)[13-16]是3D打印鈦合金的耐腐蝕性研究,文獻(xiàn)[13-23]是3D打印鈦合金的生物相容性研究。文獻(xiàn)檢索流程見圖1。
2、 結(jié)果 Results
2.1 3D打印純鈦的生物相容性研究
戴宜君等[11]研究了SLM打印技術(shù)對(duì)鈦金屬生物相容性的影響。他們采用SLM技術(shù)和傳統(tǒng)鑄造技術(shù)分別制作SLM純鈦和鑄造純鈦試樣,分別進(jìn)行細(xì)胞毒性試驗(yàn)和皮下埋植試驗(yàn),細(xì)胞毒性試驗(yàn)結(jié)果顯示SLM和鑄造組的細(xì)胞相對(duì)增值率為88.20%-101.71%,細(xì)胞毒性為1級(jí)。皮下埋植試驗(yàn)結(jié)果顯示2組金屬試件植入后,植入部位均無滲血、化膿和試件被排出的現(xiàn)象,周圍組織沒有出現(xiàn)明顯炎癥反應(yīng),無感染或壞死,且隨時(shí)間延長,組織正常生長。由此得出,采用SLM和傳統(tǒng)鑄造法制作的純鈦試件均無細(xì)胞毒性,植入大鼠體內(nèi)后不會(huì)引起明顯炎癥反應(yīng)。SLM技術(shù)不會(huì)改變純鈦的生物相容性,該工藝與傳統(tǒng)鑄造法制作的純鈦試件在生物相容性方面并無明顯差異,SLM技術(shù)可用于口腔臨床。
朱娟芳[12]利用激光快速成形技術(shù)制作純鈦植入材料,將傳統(tǒng)方法加工的純鈦?zhàn)鳛閷?duì)照組。首先分別從細(xì)胞毒性、口腔黏膜刺激、溶血、急性全身毒性和骨內(nèi)植入試驗(yàn)來評(píng)價(jià)激光快速成形純鈦的生物安全性,然后,對(duì)比觀察激光快速成形純鈦和醫(yī)用鈦在不同溶液中的金屬離子析出情況、應(yīng)力加載下的耐腐蝕情況,以及氟離子和pH值對(duì)電化學(xué)行為的影響情況等,來評(píng)價(jià)激光快速成形純鈦的耐腐蝕性。結(jié)果顯示激光快速成形純鈦的細(xì)胞毒性測(cè)試結(jié)果為0級(jí),對(duì)黏膜無刺激反應(yīng)。溶血率為2.68%,不會(huì)引起急性溶血反應(yīng)。激光快速成形純鈦浸提液注射入動(dòng)物體內(nèi)后,觀察期內(nèi)無急性毒性反應(yīng)。
骨內(nèi)埋植試驗(yàn)顯示種植體與骨組織緊密接觸。在不同溶液中,激光快速成形純鈦的鈦離子析出量均低于傳統(tǒng)方法加工的純鈦。在應(yīng)力和氟離子的共同作用下,傳統(tǒng)方法加工的純鈦比激光快速成形純鈦的腐蝕程度更嚴(yán)重。由此得出結(jié)論,激光快速成形純鈦具有優(yōu)良的生物安全性和更優(yōu)的耐電化學(xué)腐蝕及耐應(yīng)力腐蝕性能,見表1。

2.2 3D打印鈦合金的耐腐蝕性研究
趙冰凈[13]利用EBM和SLM工藝制作Ti6Al4V試件,以傳統(tǒng)鍛造試件作為對(duì)照。應(yīng)用電化學(xué)實(shí)驗(yàn)、浸泡實(shí)驗(yàn)、細(xì)胞培養(yǎng)液離子析出實(shí)驗(yàn)檢測(cè)三組試件的耐腐蝕性。電化學(xué)腐蝕實(shí)驗(yàn)結(jié)果顯示,電極電位< 1 200 mV時(shí),SLM試件的耐腐蝕性最強(qiáng);電極電位> 1 200 mV時(shí),EBM試件的耐腐蝕性最強(qiáng)。浸泡實(shí)驗(yàn)結(jié)果顯示SLM試件的耐腐蝕性最強(qiáng)。培養(yǎng)液金屬離子析出濃度顯示SLM試件Al和V離子的析出量最少, 3種試件Al和V離子的析出量均為微克級(jí),不會(huì)影響細(xì)胞黏附及增殖。證實(shí)EBM與SLM工藝制作的鈦合金試件均具有良好的耐腐蝕性。蔣軍杰[14]采用SLM技術(shù)制備TC4鈦合金塊狀試件,按打印態(tài)、退火態(tài)和軋制態(tài)合金試樣,在SBF仿生溶液和Ringer’s生理鹽液中進(jìn)行電化學(xué)測(cè)試。在SBF仿生溶液和Ringer’s生理鹽液中,SLM成型TC4合金的耐腐蝕性優(yōu)于傳統(tǒng)鑄軋工藝制備的TC4合金。王勇等[15]采用SLM技術(shù)制備TC4合金,通過電化學(xué)實(shí)驗(yàn)測(cè)試了SLM成型TC4的生物腐蝕性能。材料的自腐蝕電位和極化電阻按照軋制態(tài)、退火態(tài)、打印態(tài)的順序依次增加,證實(shí)SLM相比于傳統(tǒng)鑄軋工藝有著更好的耐蝕性能。Chen等[16]采用SLM技術(shù)制備Ti6Al4V塊體樣品,檢測(cè)了樣品分別在X、Y、Z三個(gè)平面上的耐腐蝕性,并與商業(yè)軋制鈦合金板進(jìn)行了對(duì)比,結(jié)果表明SLM鈦合金板在Y平面和Z平面具有最好的耐生物腐蝕性,優(yōu)于X平面樣品,也優(yōu)于商業(yè)軋制鈦合金板(表1)。
2.3 3D打印鈦合金的生物相容性研究
趙冰凈[13]利用
EBM和SLM工藝制作Ti6Al4V試件,以傳統(tǒng)鍛造試件作為對(duì)照,3組試件進(jìn)行體外研究;將EBM與正常組織進(jìn)行體內(nèi)研究。首先,采用掃描電鏡及細(xì)胞計(jì)數(shù)法,觀察幾種工藝試件表面骨髓基質(zhì)干細(xì)胞黏附及增殖情況,結(jié)果顯示骨髓基質(zhì)干細(xì)胞在EBM、SLM、傳統(tǒng)鍛造三種試件上的黏附增殖能力相近,細(xì)胞數(shù)量隨著培養(yǎng)時(shí)間的延長而明顯增加,細(xì)胞形態(tài)也隨著培養(yǎng)時(shí)間的延長而明顯變化。其次,采用透射電鏡觀察幾種工藝試件的骨髓基質(zhì)干細(xì)胞及比格犬皮下植入后的肝腎組織超微結(jié)構(gòu)是否損傷,結(jié)果顯示骨髓基質(zhì)干細(xì)胞及比格犬肝腎組織超微結(jié)構(gòu)與鍛造件及正常肝腎組織無明顯差別,無受損跡象。再次,采用組織學(xué)染色及大體觀察法觀察到試件周圍被一層纖維組織囊包繞,未發(fā)現(xiàn)炎癥組織及金屬顆粒。最后,采用彗星實(shí)驗(yàn)檢測(cè)比格犬皮下植入手術(shù)后的肝腎組織DNA,未發(fā)現(xiàn)受損傷。由此看出,EBM和SLM工藝制作的鈦合金試件生物相容性良好,均適合應(yīng)用到體內(nèi)。
王宏[20]采用EBM和SLM工藝制備鈦合金試樣,測(cè)試細(xì)胞毒性和溶血率,進(jìn)行皮膚刺激及皮膚致敏試驗(yàn),評(píng)價(jià)不同3D打印技術(shù)成型的鈦合金試樣的生物相容性。體外細(xì)胞試驗(yàn)結(jié)果顯示EBM和SLM兩種工藝制備的鈦合金試樣對(duì)犬骨髓間充質(zhì)干細(xì)胞的生長和成骨分化能力均沒有明顯影響。2種工藝的鈦合金試樣的溶血率分別為2.24%和2.46%,血液相容性良好。EBM和SLM成型的鈦合金試樣均對(duì)皮膚沒有刺激性和致敏性。
蔣軍杰 [14]采用SLM技術(shù)制備TC4鈦合金塊狀試件,檢測(cè)溶血率和細(xì)胞毒性。結(jié)果顯示,合金不會(huì)引起急性溶血,血液相容性優(yōu)良;細(xì)胞毒性均為0級(jí),細(xì)胞相容性良好。王勇等[15]采用SLM技術(shù)制備TC4合金,通過溶血實(shí)驗(yàn)和細(xì)胞毒性實(shí)驗(yàn)測(cè)試其生物相容性,證實(shí)SLM成型及退火后的TC4合金血液相容性優(yōu)良,兩種狀態(tài)合金的細(xì)胞毒性均為0級(jí)。張雷青[17]通過SLM 3D打印機(jī)打印出鈦合金標(biāo)準(zhǔn)試件,同時(shí)采用失蠟鑄造法制備純鈦的標(biāo)準(zhǔn)試件,利用MTT法測(cè)試試件的細(xì)胞毒性。結(jié)果顯示SLM成型鈦合金及鑄造純鈦試件均無明顯細(xì)胞毒性,都在臨床允許的范圍以內(nèi),符合牙科學(xué)對(duì)于金屬材料細(xì)胞毒性的要求。董研等[18]分別用失蠟鑄造、SLM技術(shù)制備純鈦(鑄造)/鈦合金標(biāo)準(zhǔn)試件,用MTT法測(cè)試其細(xì)胞毒性。鑄造純鈦和SLM成型鈦合金細(xì)胞毒性均為0至1級(jí),符合牙科學(xué)對(duì)于金屬材料細(xì)胞毒性的要求。
毛夢(mèng)蕓[19]用SLS制備Ti6Al4V試件,進(jìn)行體外細(xì)胞實(shí)驗(yàn)和體內(nèi)動(dòng)物實(shí)驗(yàn)。活/死細(xì)胞染色實(shí)驗(yàn)顯示細(xì)胞接種在鈦板表面24 h后黏附情況較好,活細(xì)胞數(shù)量明顯大于死細(xì)胞數(shù)量。隨著培養(yǎng)時(shí)間延長,細(xì)胞數(shù)量迅速增加,第7天時(shí)已融合90%以上。動(dòng)物實(shí)驗(yàn)顯示種植體與骨界面形成骨結(jié)合,有新生骨組織長入內(nèi)部空隙,可見大量成骨細(xì)胞及骨小梁結(jié)構(gòu)。骨結(jié)合率隨著孔隙率的升高和培養(yǎng)周期的延長而增加。證實(shí)SLS制備的Ti6Al4V試件多孔材料無細(xì)胞毒性,該材料有利于細(xì)胞黏附和增殖,有利于骨組織長入孔隙并形成良好的骨結(jié)合,具有良好的生物相容性。
Lin等[21]采用SLM和傳統(tǒng)技術(shù)制作鈦合金板,使用CCK-8測(cè)定培養(yǎng)基提取物的L929成纖維細(xì)胞的代謝情況,通過光學(xué)顯微鏡觀察其形態(tài)來評(píng)估細(xì)胞相容性,結(jié)果顯示3D打印鈦合金板的細(xì)胞相容性不低于常規(guī)板。將提取物注射到小鼠的尾靜脈中,注射后,小鼠的活動(dòng)、飲食和排泄正常。連續(xù)4 d測(cè)量小鼠的體質(zhì)量變化,都沒有出現(xiàn)顯著差異,說明樣品無急性全身毒性。最后,將其植入兔的背部肌肉來研究組織相容性,植入后兔子的傷口愈合都很好,沒有觀察到組織損傷或炎癥改變。
體外結(jié)果表明3D打印鈦合金板的細(xì)胞相容性與常規(guī)板相似。體內(nèi)數(shù)據(jù)也證實(shí)了兩種制造技術(shù)的組織相容性類似。總之,體內(nèi)和體外實(shí)驗(yàn)都表明3D打印鈦合金板材具有良好的生物相容性。
Tan等[22]通過SLM和EBM方法制造Ti6Al4V支架,通過體外研究和體內(nèi)研究評(píng)價(jià)了其生物相容性,提出金屬3D打印在生物醫(yī)學(xué)領(lǐng)域具有極高的潛力。Yang等[23]通過激光束熔化3D 打印技術(shù)制造3 種孔徑的多孔Ti6Al4V植入物模型。對(duì)于體外研究,進(jìn)行植入物的生物相容性和成骨能力試驗(yàn),結(jié)果表明樣品在細(xì)胞生長、遷移和黏附方面表現(xiàn)出很好的生物相容性(表1)。
3、 討論 Discussion
醫(yī)用材料對(duì)于生物性能的要求極高,生物相容性是醫(yī)用材料應(yīng)用于人體后與機(jī)體之間發(fā)生相互作用,醫(yī)用材料與人體機(jī)體對(duì)相互作用的反應(yīng)能力能夠保持相對(duì)穩(wěn)定而不會(huì)相互排斥[24]。金屬鈦具有同素異構(gòu)相轉(zhuǎn)變,可由低溫α相轉(zhuǎn)變?yōu)楦邷卅孪唷T缭?0世紀(jì)40年代初期,Bothe等首先把純鈦引入到生物醫(yī)學(xué)領(lǐng)域,隨后,Branemark將純鈦用于口腔種植體后,純鈦?zhàn)鳛橥饪浦踩爰牧系玫酱蠓秶鷳?yīng)用。純鈦等α型鈦合金雖然在生理環(huán)境中抗腐蝕性能優(yōu)良,但其強(qiáng)度較低、耐磨性較差,從而限制了骨科領(lǐng)域的使用。α+β型鈦合金Ti6Al4V強(qiáng)度較高,綜合加工性能優(yōu)異,在20世紀(jì)70年代后期已經(jīng)被廣泛用于制作外科修復(fù)或替換材料[25-26]。
傳統(tǒng)工藝制作的鈦及鈦合金已經(jīng)是應(yīng)用非常成熟的生物醫(yī)學(xué)材料,在復(fù)雜及個(gè)性化鈦及鈦合金醫(yī)療器械加工與制造過程中,也逐漸開始運(yùn)用金屬3D打印技術(shù)。
3D打印憑借著加工成形能力強(qiáng)、實(shí)現(xiàn)個(gè)性化定制、加工周期短、成本降低[27]、可打印材料范圍廣泛[28]、尺寸精度較高等優(yōu)勢(shì)[29],無疑已成為研究熱點(diǎn)。在上述研究中,對(duì)于純鈦和鈦合金,不同學(xué)者分別采用SLS、SLM、EBM技術(shù)和傳統(tǒng)鑄造法制作試件進(jìn)行耐腐蝕性實(shí)驗(yàn)、細(xì)胞毒性實(shí)驗(yàn)、皮下埋植實(shí)驗(yàn)、口腔黏膜刺激實(shí)驗(yàn)、溶血試驗(yàn)、急性全身毒性試驗(yàn)、骨內(nèi)植入試驗(yàn)等,證實(shí)3D打印和鑄造法制作的鈦及鈦合金試件都具有良好的生物安全性,且在某些條件下,3D打印試件的性能更優(yōu)于傳統(tǒng)鑄 軋[11-23]。3D打印技術(shù)不會(huì)改變材料的生物安全性,利用該技術(shù)的優(yōu)勢(shì),鈦及鈦合金在牙科及骨科等個(gè)性化醫(yī)療領(lǐng)域?qū)?huì)有更好的應(yīng)用前景。
在牙科領(lǐng)域,3D打印技術(shù)能夠進(jìn)行定制化加工,可以生產(chǎn)精密個(gè)性化修復(fù)體,臨床應(yīng)用效果最佳,比傳統(tǒng)牙床材料具有突出優(yōu)勢(shì)[30],該技術(shù)在制作牙科支架、冠橋方面已經(jīng)應(yīng)用的較為成熟。在骨科領(lǐng)域,多孔鈦及鈦合金抗腐蝕性能、生物相容性以及與人骨相匹配的力學(xué)性能都非常優(yōu)異,是人體理想的骨科替代植入件[31]。采用SLM或者EBM技術(shù)制作的椎間融合器、髖關(guān)節(jié)以及其他骨科植入物均獲得了較好的臨床效果。2015年9月國內(nèi)第一個(gè)3D打印人體植入物——人工髖關(guān)節(jié)獲得國家食品藥品監(jiān)督管理總局的注冊(cè)批準(zhǔn)[10],上市之后該類產(chǎn)品收入增長迅速。2016年5月和7月,多孔型金屬骨科植入材料椎體假體和椎間融合器分別獲準(zhǔn)注冊(cè)。2018年2月,個(gè)體化下頜骨重建假體也通過注冊(cè)審批,正式進(jìn)入市場。與此同時(shí),國內(nèi)多家企業(yè)的多款金屬3D打印定制化髖臼杯、胸腰椎融合體、股骨部件、長段骨修復(fù)體、定制融固系統(tǒng)、膝關(guān)節(jié)假體、腕關(guān)節(jié)假體、肩關(guān)節(jié)假體、骨盆假體等產(chǎn)品也在緊鑼密鼓的進(jìn)行臨床試驗(yàn),未來1或2年內(nèi)有望獲批上市。國外早在2007年就有3D打印髖臼杯產(chǎn)品通過CE認(rèn)證,之后陸續(xù)有3D打印鈦產(chǎn)品通過CE和FDA認(rèn)證[10]。近幾年,F(xiàn)DA批準(zhǔn)注冊(cè)的3D打印產(chǎn)品包括定制化鈦金屬顱面植入物、頸椎植入物、脊柱植入物、鈦金屬骶髂關(guān)節(jié)、腰椎骨盆等。這充分肯定了3D打印鈦合金產(chǎn)品在醫(yī)療領(lǐng)域的應(yīng)用前景。
多孔鈦材料獨(dú)特的多孔結(jié)構(gòu)及粗糙的內(nèi)外表面將有利于成骨細(xì)胞的黏附、增殖和分化,促使新骨組織長入孔隙,有利于植入體同骨之間形成一個(gè)整體[26,32]。
傳統(tǒng)加工方式很難成型結(jié)構(gòu)如此復(fù)雜的多孔鈦材料,3D打印可以有效解決這個(gè)問題。當(dāng)然,多孔鈦商業(yè)化應(yīng)用也面臨著一些難題,如如何實(shí)現(xiàn)孔徑、孔隙率和力學(xué)性能間的最佳匹配,如何清除孔隙中殘留粉末,是否會(huì)有殘留毒性,這些都需要進(jìn)行大量深入的科學(xué)基礎(chǔ)研究[26,33]。再加上器械體積、打印速度、金屬粉末價(jià)格、以及端到端的設(shè)計(jì)、制造、組裝、運(yùn)輸、銷售和操作等瓶頸,也制約了3D打印技術(shù)的廣泛應(yīng)用。這些問題,有望在未來不斷地研發(fā)創(chuàng)新中獲得突破。
通過眾多學(xué)者前期的試驗(yàn)研究,鈦及其合金可以很好的適應(yīng)生物環(huán)境,未來醫(yī)用鈦及鈦合金的發(fā)展趨勢(shì)正向著整體材料及表面狀態(tài)多尺度設(shè)計(jì)、優(yōu)化自身組織結(jié)構(gòu)、調(diào)控力學(xué)性能、實(shí)現(xiàn)表面功能化方面發(fā)展,要實(shí)現(xiàn)這些,無疑要大力發(fā)展先進(jìn)的材料加工制造技術(shù),3D打印必將會(huì)扮演越來越重要的角色[25]。3D打印鈦及鈦合金具有良好的生物安全性,且可以設(shè)計(jì)、調(diào)控材料自身結(jié)構(gòu)和優(yōu)化性能,相比傳統(tǒng)的鑄造工藝,3D打印具有明顯優(yōu)勢(shì),該技術(shù)將極大的推動(dòng)鈦合金產(chǎn)品在個(gè)性化醫(yī)療領(lǐng)域的廣泛應(yīng)用。
由于3D打印技術(shù)有不同的成型原理,各種技術(shù)受能量來源、成型方式、工藝參數(shù)等的影響,在實(shí)際應(yīng)用中,有必要根據(jù)具體情況對(duì)3D打印的成型方式、工藝參數(shù)等進(jìn)行調(diào)整、優(yōu)化和改進(jìn)。3D打印制造技術(shù)雖然短時(shí)間內(nèi)還不能與傳統(tǒng)制造并駕齊驅(qū),但它正被應(yīng)用于醫(yī)療器械原型制作、零部件以及直接制作高度定制或工藝復(fù)雜但產(chǎn)量較少的器械物件等。隨著原材料、制造設(shè)備、關(guān)鍵工藝技術(shù)等方面的不斷突破,3D打印技術(shù)在醫(yī)療器械領(lǐng)域的應(yīng)用將越來越廣泛。
致謝:衷心感謝成都優(yōu)材科技有限公司領(lǐng)導(dǎo)同事們給予的熱情幫助和耐心解惑。
作者貢獻(xiàn):文章資料收集、成文由吳利蘋完成,審校、修改由鄒善方、劉睿誠完成,審核、批準(zhǔn)由曾益?zhèn)ネ瓿伞?/p>
經(jīng) 費(fèi) 支 持 : 該 文 章 接 受 了 “ 四 川 省 科 技 廳 重 點(diǎn) 研 發(fā) 項(xiàng) 目(2018GZ0298)”的資助。所有作者聲明,經(jīng)費(fèi)支持沒有影響文章觀點(diǎn)和對(duì)研究數(shù)據(jù)客觀結(jié)果的統(tǒng)計(jì)分析及其報(bào)道。
利益沖突:文章的全部作者聲明,在課題研究和文章撰寫過程中不存在利益沖突。
機(jī)構(gòu)倫理問題:未涉及倫理沖突的內(nèi)容。
寫作指南:該研究遵守國際醫(yī)學(xué)期刊編輯委員會(huì)《學(xué)術(shù)研究實(shí)驗(yàn)與報(bào)告和醫(yī)學(xué)期刊編輯與發(fā)表的推薦規(guī)范》。
文章查重:文章出版前已經(jīng)過 CNKI 反剽竊文獻(xiàn)檢測(cè)系統(tǒng)進(jìn)行 3 次查重。
文章外審:文章經(jīng)國內(nèi)小同行外審專家雙盲外審,符合本刊發(fā)稿宗旨。
生物統(tǒng)計(jì)學(xué)聲明:未涉及生物統(tǒng)計(jì)學(xué)。
文章版權(quán):文章出版前雜志已與全體作者授權(quán)人簽署了版權(quán)相關(guān)協(xié)議。
開放獲取聲明:這是一篇開放獲取文章,根據(jù)《知識(shí)共享許可協(xié)議》“署名-非商業(yè)性使用-相同方式共享3.0”條款,在合理引用的情況下,允許他人以非商業(yè)性目的基于原文內(nèi)容編輯、調(diào)整和擴(kuò)展,同時(shí)允許任何用戶閱讀、下載、拷貝、傳遞、打印、檢索、超級(jí)鏈接該文獻(xiàn),并為之建立索引,用作軟件的輸入數(shù)據(jù)或其它任何合法用途。
4、 參考文獻(xiàn) References
[1]賈翃,逯福生,郝斌. 2016年中國鈦工業(yè)發(fā)展報(bào)告[J]. 鋼鐵釩鈦,2017,34(2):1-7.
[2]韓建業(yè),羅錦華,袁思波,等.口腔用鈦及鈦合金材料的研究現(xiàn)狀[J].鈦工業(yè)進(jìn)展, 2016,33(3):1-7.
[3]梁銳英,李長義,張連云.齒科用鈦合金的研究進(jìn)展[J]. 國外醫(yī)學(xué)(口腔醫(yī)學(xué)分冊(cè)), 2006,33(1):45-47.
[4]謝輝,張玉勤,孟增東,等.鈦合金特性及其在骨科領(lǐng)域的應(yīng)用現(xiàn)狀和研究進(jìn)展[J].生物骨科材料與臨床研究, 2013,10(6):29-32.
[5]張文毓.生物醫(yī)用鈦合金的研究進(jìn)展[J].化學(xué)與黏合. 2014,36(5):369-373.
[6]陳光霞.可摘除局部義齒支架激光快速成型技術(shù)與設(shè)備研究[D].武漢:華中科技大學(xué), 2009.
[7]陳克南. SLM 3D打印純鈦冠金瓷結(jié)合與適合性的基礎(chǔ)和臨床研究[D].西安:第四軍醫(yī)大學(xué), 2016.
[8]劉一帆,王偉娜,于海,等.選擇性激光熔覆(SLM)鈦合金可摘局部義齒支架的適合性研究[J].實(shí)用口腔醫(yī)學(xué)雜志, 2017,33(3):302-305.
[9]陳光霞,曾曉雁,王澤敏,等.可摘除局部義齒支架的選擇性激光熔化制造技術(shù)[J]. 現(xiàn)代制造工程, 2010(6):64-68.
[10] 趙丹妹,王春仁,韓倩倩,等.3D打印醫(yī)用鈦合金植入物的研究現(xiàn)狀與進(jìn)展[J].中國醫(yī)療器械信息, 2017,23(3):1-5.
[11] 戴宜君,董研,周東,等.SLM打印技術(shù)對(duì)鈷鉻及鈦金屬生物相容性的影響[C].第十一次全國口腔修復(fù)學(xué)學(xué)術(shù)會(huì)議論文. 2017:33-34.
[12] 朱娟芳.激光快速成形技術(shù)制作純鈦植入材料的實(shí)驗(yàn)研究[D].西安:第四軍醫(yī)大學(xué), 2007.
[13] 趙冰凈.3D打印Ti-6Al-4V理化性能及生物相容性研究[D]. 北京:中國人民解放軍醫(yī)學(xué)院, 2016.
[14] 蔣軍杰.選區(qū)激光熔化成型醫(yī)用Ti-6Al-4V合金的組織和性能研究[D].重慶:重慶大學(xué), 2015.
[15] 王勇,蔣軍杰,喬麗英,等.選區(qū)激光熔化TC4生物腐蝕和生物相容性分析[J].重慶大學(xué)學(xué)報(bào), 2015,38(3):21-27.
[16] Chen LY, Huang JC, Lin CH, et al.. Anisotropic response ofTi-6Al-4V alloy fabricated by 3D printing selective lasermelting. Mater Sci Eng A. 2017;682:389-395.
[17] 張雷青.基于數(shù)字化設(shè)計(jì)和3D打印的頜骨缺損贗復(fù)體修復(fù)及3D打印金屬材料細(xì)胞毒性的初步研究[D].杭州:浙江大學(xué), 2016.
[18] 董研,彭偉,張雷青,等.基于選擇性激光熔融技術(shù)的贗復(fù)體支架打印及金屬試件細(xì)胞毒性的研究[C].第十一次全國口腔修復(fù)學(xué)學(xué)術(shù)會(huì)議論文.2017:55.
[19] 毛夢(mèng)蕓.選擇性激光燒結(jié)制備多孔鈦的機(jī)械性能與生物相容性研究[D].濟(jì)南:山東大學(xué),2016.
[20] 王宏. 應(yīng)用個(gè)性化鈦合金修復(fù)體和同種異體下頜骨修復(fù)比格犬下頜骨缺損的比較研究[D].北京:中國人民解放軍醫(yī)學(xué)院, 2017.
[21] Lin X, Xiao X, Wang Y, et al. Biocompatibility of Bespoke3D-Printed Titanium Alloy Plates for Treating AcetabularFractures. Biomed Res Int. 2018;2018:2053486.
[22] Tan XP, Tan YJ, Chow CSL, et al. Metallic powder-bed based3D printing of cellular scaffolds for orthopaedic implants: Astate-of-the-art review on manufacturing, topological design,mechanical properties and biocompatibility. Mater Sci Eng CMater Biol Appl. 2017;76:1328-1343.
[23] Yang F, Chen C, Zhou Q, et al. Laser beam melting 3Dprinting of Ti6Al4V based porous structured dental implants:fabrication, biocompatibility analysis and photoelastic study.Sci Rep. 2017;7:45360.
[24] 于華,張曉東,王亦菁,等.口腔金屬材料安全性?相容性以及功能性的評(píng)價(jià)[J].中國組織工程研究, 2012,16(47):8907-8914.
[25] 于振濤,余森,張明華,等.外科植入物用新型醫(yī)用鈦合金材料設(shè)計(jì)?開發(fā)與應(yīng)用現(xiàn)狀及進(jìn)展[J].中國材料進(jìn)展, 2010,29(12):35-51.
[26] 于振濤,余森,程軍,等.新型醫(yī)用鈦合金材料的研發(fā)和應(yīng)用現(xiàn)狀[J].金屬學(xué)報(bào), 2017,53(10):1238-1264.
[27] 羅麗娟,余森,于振濤,等. 3D打印鈦及鈦合金醫(yī)療器械的優(yōu)勢(shì)及臨床應(yīng)用現(xiàn)狀[J].生物骨科材料與臨床研究,2015,12(6):72-75.
[28] 任繼文,劉建書.選擇性激光燒結(jié)主要成型材料的研究進(jìn)展[J].機(jī)械設(shè)計(jì)與制造, 2010,48(11):266-268.
[29] Venkatesh KV, Nandini VV. Direct metal laser sintering: adigitised metal casting technology. J Indian Prosthodont Soc.2013;13(4):389-392.
[30] 譚兆軍,郭亞峰.口腔修復(fù)用鈦及鈦合金的理化特性及其生物相容性[J].中國組織工程研究與臨床康復(fù), 2008,12(19):3721-3724.
[31] 李洋,陳長軍,王曉南,等.醫(yī)用多孔鈦及鈦合金的研究進(jìn)展[J].現(xiàn)代制造工程, 2015(7):144-148.
[32] Tian Y, Yu Z, Ong CY, et al. Microstructure, elasticdeformation behavior and mechanical properties ofbiomedical β-type titanium alloy thin-tube used for stents. JMech Behav Biomed Mater. 2015;45:132-141.
[33] Butscher A, Bohner M, Hofmann S, et al. Structural andmaterial approaches to bone tissue engineering inpowder-based three-dimensional printing. Acta Biomater.2011;7(3):907-920.
相關(guān)鏈接









